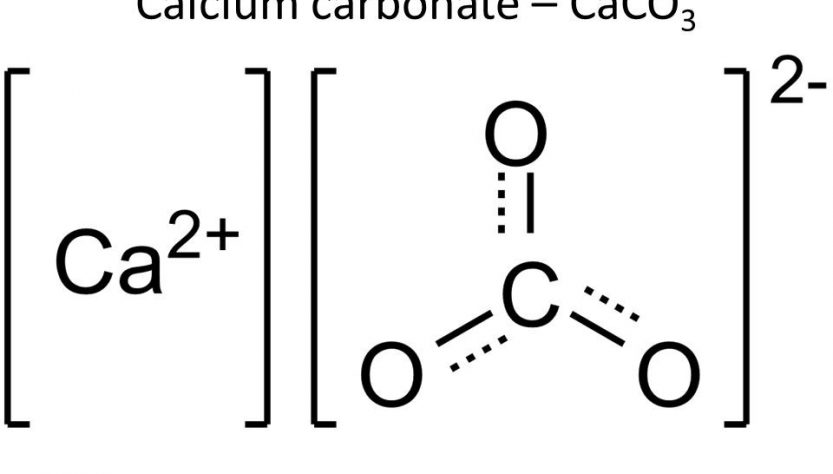
CaCO3 + 2HCl → H2O + CO2 + CaCl2 Cách viết phương trình phản ứng hóa học cân bằng như thế nào? thì ở dưới bài viết này chúng ta cùng nhau đi tìm hiểu nhé. Để vận dụng vào làm bài tập một cách chính xác và hiệu quả nhất.
Xem thêm Các phương trình phản ứng hóa học:
- 3CO +Fe2O3 ⟶ 2Fe+3CO2
- C6H12O6 → 2C2H5OH + 2CO2
- 2C2H5OH + 2CO2 → C6H12O6
- 2CO2 → 2CO + O2
- CaCO3 → CaO + CO2↑
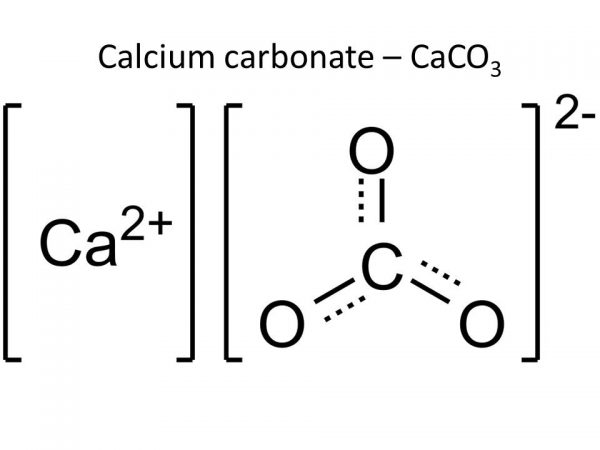
Phương trình phản ứng CaCO3 ra CaCl2:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Trong đó :
- CaCO3 là canxi cacbonat Calcium carbonate ( là một chất rắn có màu trắng )
- HCl là axit clohidric ( là một dung dịch axit không màu )
- CaCl2 là Canxi diclorua calcium chloride ( là một dung dịch có màu trắng )
- CO2 là Cacbon dioxit Carbon dioxide ( là một chất khí không có màu )
- H2O là nước ( là một chất lỏng không có màu )
Điều kiện phản ứng CaCO3 ra CaCl2
Nhiệt độ thường
Thực hiện phương trình phản ứng :
Cho CaCO3 tác dụng với dung dịch Axit HCl, khi hiện tượng xảy ra ta thấy có Chất rắn màu trắng Canxi cacbonat (CaCO3) tan dần và sinh ra khí Cacbonic (CO2) làm sủi bọt dung dịch.
Thông tin thêm :
Tương tự như CaCO3, các muối cacbonat tan trong dung dịch HCl tạo thành muối mới và giải phóng khí CO2.Axit clohiđric là axit mạnh có khả năng tác dụng với muối. CO2 được điều chế bằng cách cho dung dịch HCl tác dụng với đá vôi.
Khái quát về CaCl2:
Clorua canxi (CaCl2) hay canxi clorua , là hợp chất ion của canxi và clo. Chất này tan nhiều trong nước.
Tại nhiệt độ phòng, nó là chất rắn.
Chất này có thể sản xuất từ đá vôi nhưng đối với việc sản xuất sản lượng lớn thì người ta tạo nó như là một sản phẩm phụ của công nghệ Solvay.
Do nó có tính hút ẩm cao,người ta phải chứa muối này trong các dụng cụ đậy nắp kín.

CaCl2 được sử dụng rất đa dạng như : công nghiệp, thực phẩm, sinh học , Y học…………Ngoài ra CaCl2 còn ngăn ngừa :
-Calci chloride có thể gây dị ứng, cụ thể là trên da ẩm. Đeo găng tay và kính hay mặt nạ che phủ toàn phần để bảo vệ tay và mắt; tránh hít thở phải hơi hay bụi chứa calci chloride.
-Calci chloride khan phản ứng tỏa nhiệt khi tiếp xúc với nước. Các vết bỏng có thể sinh ra tại miệng hay thực quản nếu vô tình nuốt phải các viên calci chloride khan. Trẻ nhỏ dễ bị tổn thương hơn người trưởng thành do chưa có kinh nghiệm tránh các thức ăn nóng, vì thế các viên calci chloride cần phải để xa nơi tầm với của chúng.