Phương trình điều chế axit clohiric, khi cho muối ăn (NaCl rắn) tác dụng với axit sunfuric đặc ở nhiệt độ thích hợp tạo ra muối NaHSO4, Viết phương trình hóa học đã cân bằng H2SO4 + 2NaCl → 2HCl + Na2SO4. Đây là thông tin về phương trình hóa học điều chế ra HCl, Hi vọng sẽ giúp ích được cho các bạn đọc cũng như các em học có kiến thức cơ bản để vận dụng vào làm bài tập cũng như trong phòng thí nghiệm.
Nội dung tham khảo thêm các phương trình phản ứng khác :
Phương trình hóa học đã được cân bằng :
| H2SO4 | + | 2NaCl | → | 2HCl | + | Na2SO4 |
| axit sulfuric | Natri Clorua | axit clohidric | natri sulfat | |||
| dung dịch không màu | dung dịch màu trắng | dung dịch không màu | chất rắn có màu trắng | |||
| axit | muối | axit | muối |
Điều kiện phản ứng H2SO4 ra HCl
Nhiệt độ: > 400
Cách thực hiện phương trình phản ứng :
Cho tinh thể NaCl tác dụng với axit H2SO4 đậm đặc và đun nóng rồi hấp thụ vào nước để thu được dung dịch axit clohiđric
Bạn có biết: Phương pháp điều chế hiđro clorua trong phòng thí nghiệm
Các phương trình điều chế HCl :
HCN + C2H5Cl ⟶ HCl + C2H5CN
H2O + ICl ⟶ HCl + HIO
HClO2 + HClO ⟶ HCl + HClO3
Na2SO3 + HClO ⟶ HCl + Na2SO4
NaCl + H2SO4 -<250oC→ NaHSO4 + HCl↑
Nguồn gốc của NaCl Natri Clorua
– Khả năng bảo quản thực phẩm của muối là cơ sở của các nền văn mình. Giúp con người thời xưa bớt phụ thuộc vào nguồn thực phẩm theo mùa
– Thời trung cổ, muối NaCl còn được dùng làm đơn vị để mua bán, trao đổi nô lệ
– Đầu thế kỷ XX, muối vẫn là động cơ chủ yếu trong hoạt động nền kinh tế
– Người Nhật theo tín ngưỡng Shinto cho rằng, muối được coi là sự “tinh khiết” và được sử dụng trong nghi thức ban phước cho con người và các địa điểm
– Trong Kinh thánh, có 32 chỉ dẫn liên quan đến muối và nổi tiếng nhất trong số đó có lẽ là câu chuyện về một người đàn bà bị biến thành cột muối khi không nghe lời các thiên sứ.
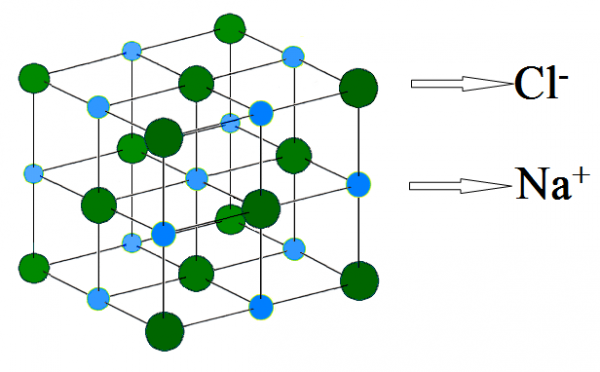
Tính chất hoá học của NaCl Natri Clorua
– Phản ứng nhiệt phân
2NaCl → Cl2 + 2Na
sinh ra chất rắn Na màu trắng và khí Cl2 màu vàng đục
AgNO3 + NaCl → AgCl + NaNO3
Nhỏ vài giọt dung dịch bạc nitrat AgNO3 vào ống nghiệm có sẵn 1ml dung dịch NaCl thì xuất hiện kết tủa trắng và 2 muối mới.
– Phản ứng Oxy hóa khử
2H2O + 2NaCl → Cl2 + H2 + 2NaOH
điều kiện là Điện phân có màng ngăn và xuất hiện khí thoát ra
– Tác dụng với axit H2SO4 đậm đặc
H2SO4 + NaCl → HCl + NaHSO4
phản ứng thu được axit HCl
– NaCl có kết tủa không?
Câu trả lời là Có. Muối ăn – NaCl kết tủa dạng tinh thể màu trắng do có lẫn MgCl2 và CaCl2