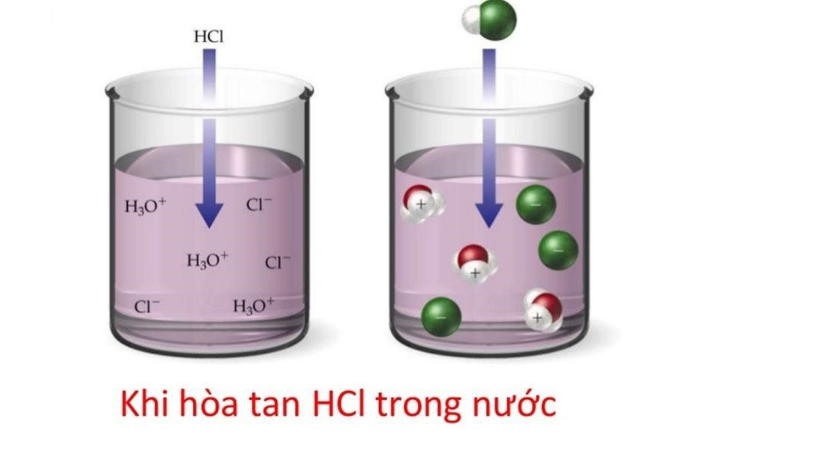
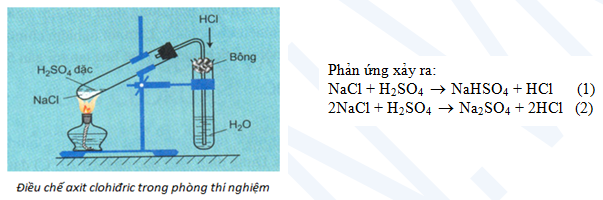
axit clohidric có đầy đủ những tính chất hóa học chung của axit không? nó có những tính chất gì khác với các axit khác. Axit clohidric (HCl) là hóa chất có vai trò rất quan trọng trong đời sống hàng ngày, được sử dụng làm nguyên liệu hoặc chất xúc tác trong nhiều ngành công nghiệp sản xuất khác nhau, chúng ta cùng đi tìm hiểu về chất axit này nhé :
Axit HCl- thông tin tổng quan
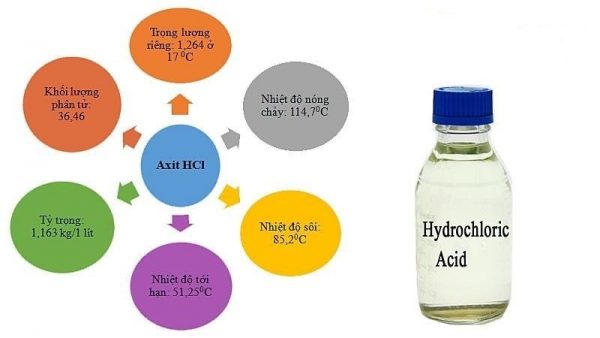
Axit HCl (Axit Clohydric) có tên gọi khác là axit muriatic, được phát hiện từ thời phục hưng trong muối ăn và tồn tại, phát triển đến nay.
Axit HCl là một axit đơn, có thể phân rã trong môi trường nước. Ở nhiệt độ thường, dung dịch axit này không màu, hoặc hơi ngả vàng nếu lẫn tạp chất. Có thể bốc hơi, khúc xạ với ánh sáng. Nó được ứng dụng nhiều nhất trong công nghiệp sinh học.
Tên gọi: Hydrogen clorua (khí); Axit clohidric (dung dịch)
Tên hóa học (IUPAC): Hydrogen clorua (khí); Axit clohiđric (dung dịch)
Công thức phân tử: HCl
Tính chất hoá học của axit clohiđric HCl
Dung dịch HCl có đầy đủ tính chất của một axit mạnh
1. Làm quỳ tím chuyển thành màu đỏ.
2. HCl tác dụng với kim loại
HCl tác dụng kim loại đứng trước H tạo thành muối và khí hidro
Fe + 2HCl → FeCl2 + H2↑
6HCl + 2Al → 2AlCl3 + 3H2↑
2HCl + Mg → MgCl2 + H2↑
3. HCl tác dụng với oxit kim loại
HCl tác dụng oxit kim loại tạo thành muối và nước
6HCl + Al2O3 →2AlCl3 + 3H2O
Fe3O4 + 8HCl → 4H2O + FeCl2+ 2FeCl3
2HCl + CuO → CuCl2 + H2O
4. HCl tác dụng với bazơ.
HCl tác dụng bazơ dung dịch hoặc bazơ rắn tạo thành muối và nước
3HCl + Al(OH)3 → AlCl3 + 3H2O
2HCl + 2NaOH → 2NaCl + H2O
2HCl + Ca(OH)2 → CaCl2 + 2H2O
2HCl + Fe(OH)2 → FeCl2 + 2H2O
5. HCl tác dụng với muối
HCl tác dụng muối tạo thành muối và axit mới
*Điều kiện: tạo kết tủa, khí bay lên hoặc axit mới yếu hơn
K2CO3 + 2HCl → 2KCl + H2O + CO2↑
2HCl + BaS → BaCl2 + H2S↑
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + 2HCl → AgCl↓ + HNO3
6. HCl tác dụng với hợp chất có tính oxi hóa
Ngoài tính oxi hóa khi tác dụng với các kim loại đứng trước H2 , HCl còn đóng vai trò chất khử khi tác dụng với chất có tính oxi hóa mạnh như KMnO4, K2Cr2O7, MnO2, KClO3, …
6HCl + KClO3 → KCl + 3Cl2↑ + 3H2O
2HCl + MnO2 → MnCl2 + Cl2↑ + H2O
14HCl + K2Cr2O7 → 2KCl + 2CrCl3 + 3Cl2↑ + 7H2O
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
Nhiệt độ sôi của nước? tính chất vật lý của nước

Ứng dụng của Axit Clohidric trong đời sống
Giúp để tẩy gỉ thép để loại bỏ gỉ trên thép bằng nồng độ Axit HCL 18% là phổ biến:
Fe2O3 + Fe + 6 HCl → 3 FeCl2 + 3 H2O
Giúp sản xuất các hợp chất hữu cơ như vinyl clorua và dicloroetan để sản xuất PVC hoặc than hoạt tính:
2 CH2=CH2 + 4 HCl + O2 → 2 ClCH2CH2Cl + 2 H2O
gỗ + HCl + nhiệt → than hoạt tính
Giúp sản xuất các hợp chất vô cơ theo phản ứng axit-bazơ.
Sử dụng làm chất keo tụ và chất đông tụ để làm lắng các thành phần trong quá trình xử lý nước thải, sản xuất nước uống, sản xuất giấy cũng như mạ điện cho công nghiệp mạ và sản xuất pin.
Giúp kiểm soát và trung hòa PH cụ thể là điều chỉnh tính bazơ trong dung dịch:
OH− + HCl → H2O + Cl−
Dùng để rửa các cation từ các loại nhựa để giúp các loại nước đã được khử khoáng.
Ứng dụng trong tất cả các ngành công nghiệp hóa, sản xuất nước uống và một số ngành công nghiệp thực phẩm.
Ứng dụng trong sản xuất thực phẩm: Các sản phẩm đặc trưng như aspartame, fructose, axít citric, lysine, thủy phân protein thực vật, và trong sản xuất gelatin.
Các ứng dụng khác của HCl như: xử lý da, vệ sinh nhà cửa, xây dựng nhà…
Những quy định cần nhớ khi sử dụng, bảo quản axit clohydric HCl
1. Sử dụng axit clohydric HCl đảm bảo an toàn
Khi tiếp xúc với Axit clohydric phải mang đầy đủ trang bị bảo hộ lao động như ủng gang tay cao su khẩu trang, kính bảo hộ, mặt nạ…
Khi bị Axit clohidric bắn vào da, phải nhanh chóng dùng nước xối nhiều lần cho đến khi hết cảm giác ngứa đối với da hoặc phải đưa đến cơ sở y tế.
Nếu như axit clric bị rơi vãi ra ngoài thì nên xối nhiều nước để rửa sạch hóa chất trên bề mặt…
2. Cách bảo quản axit clohyric HCl 35%, HCl 30% hiệu quả
Phải bảo quản axit tại nơi khô thoáng được che mưa nắng, cân có các biện pháp để tránh các nguy cơ gây nên đỗ vỡ và rò rỉ hóa chất ra ngoài.
Nền kho chứa phải làm bằng vật liệu chịu axit.
Tuyệt đối không bảo quản chung với các chất dễ cháy, các chất oxy hóa, không để axit tiếp tục với các loại kim loại.
Không để can phi chứa axit chồng lên nhau khi bảo quản.
xem thêm :
Hidro clorua là gì? cấu tạo phân tử và tính chất của Hcl