Để hiểu rõ những chất nào có thể tác dụng được với nhau, Mối liên hệ giữa chúng như thế nào? để Viết được phương trình của các chất. Hôm nay chúng tôi sẽ hướng dẫn các bạn cách tìm mối liên hệ giữ H+ chất phản ứng và sản phẩm chất khử NO3-, Mời các bạn cùng đón đọc để tìm hiểu tài liệu một cách chính xác.
Lưu ý :
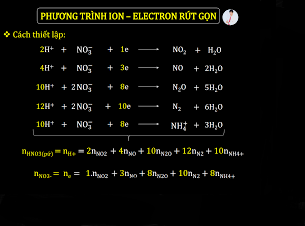
Công thức mối liên hệ giữa H+ chất sản phẩm và Sản phẩm khử NO3- :
4H+ + NO3 – + 3e —> NO + 2H2O
2H+ + NO3 – + 1e —> NO2 + 2H2O
10H+ + NO3 – + 8e —> NH4 + 3H2O
12H+ + 2NO3 – + 10e —> N2 + 6H2O
10H+ + 2NO3 – + 8e —> N2O + 5H2O
Ở tất cả các phản ứng trên, Nếu còn H+ dư và còn kim loại đứng trước H thì
2H+ + 2e —> H2
Các hỗn hợp chất khử chứa các oxit thì tốn thêm H+ để chuyển phần oxi trong oxit này thành H2O :
2H+ + O —> H2O
Vậy : nH+ = 2nNO2 + 4nNO + 10nN2O + 12nN2 + 10nNH4 + 2nH2 + 2nO trong oxít
Lưu ý :
Vấn đề về muối Fe3+, Fe2+ trong dung dịch sau phản ứng hiện có 2 vấn đề cần lưu ý :
Vấn đề 1 :
Khí H2 thì dung dịch không có Fe3+ lý do là theo dãy điện hóa, Fe3+ có tính oxi hóa mạnh hơn H+ nên Fe3+ sẽ bị khử trước H+ vì vậy khi H+ bị khử sinh ra H2 thì Fe3+ đã hết từ trước đó rồi.
Vấn đề 2 :
Khí H2 thì dung dịch vẫn có thể có Fe3+. Lý do là chất rắn ban đầu đem hòa tan vào H+, NO3- thì một phần oxit như Fe2O3, Fe3O4 có thể tan trong H+ sau khi chất khử ( Mg, Al, Zn, Fe..) đã hết.
Nhận xét :
Ở vấn đề 1 chỉ dùng khi có Fe3+ đã có sẵn nhưng nếu không có sẵn Fe3+ không có sẵn thì Fe2O3, Fe3O4 cần lưu ý thêm hai oixt này chứa Fe+ 3 chưa không phải là Fe3+ nó cần phản ứng với H+mới chuyển thành ion thì vấn đề 2 lại phù hợp với thực tế, và không trái quy luật nào.
Hi vọng bài viết này đem lại nhiều kiến thức mà bạn chưa tìm hiểu được, nhờ đó các bạn có thể chọn chính xác được các chất khi tham gia phản ứng của chất khử cũng như chất tham gia. Các bạn có thể tham khảo thêm các bài viết khác của chúng tôi, Xin cảm ơn.