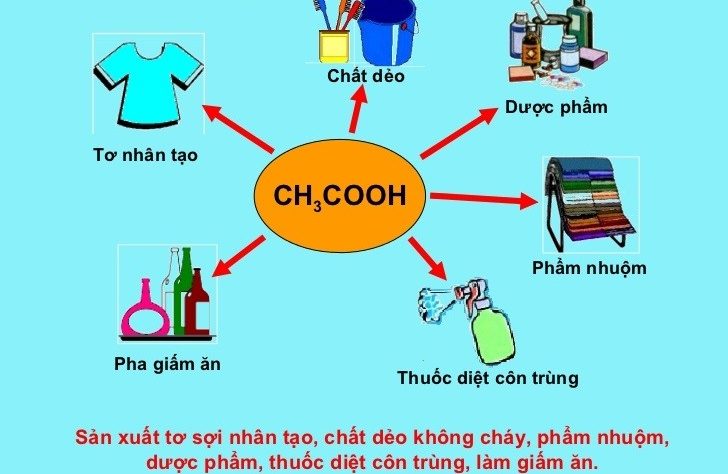
CH3COOH là gì? Đó chính là công thức hóa học của axit axetic, một loại axit được sử dụng rộng rãi trong cuộc sống hàng ngày, đặc biệt là lĩnh vực ẩm thực, nấu ăn dưới tên gọi là “giấm”. Vậy CH3COOH có những tính chất gì? phương trình phản ứng của CH3COOH tạo ra CO2 là gì? hãy cùng chúng tôi đi tìm hiểu về PTPƯ của axit axetic nhé.
Axit axetic ( CH3COOH ) có thể tạo các phản ứng hóa học đặc trưng của nhóm axit cacboxylic như tạo ra nước và ethanoat kim loại khi phản ứng với kiềm; tạo ra ethanoat kim loại khi phản ứng với kim loại; và tạo ra ethanoat kim loại, nước và cacbon dioxide khi phản ứng với các cacbonat và bicacbonat. Phản ứng đặc trưng nhất là tạo thành ethanol, và tạo thành các dẫn xuất như axetyl chloride bằng cách thay thế nhóm -OH bởi -Cl. Các dẫn xuất thay thế khác như anhydride axetic; anhydride này được tạo ra theo phản ứng trùng ngưng tách phân tử nước từ hai phân tử của axit axetic. Các este của axit axetic tương tự có thể được tạo ra bởi este hóa, và các amit. Khi nung trên 440 °C, axit axetic phân hủy tạo ra cacbon dioxide và metan, hoặc tạo ra ethenon và nước.
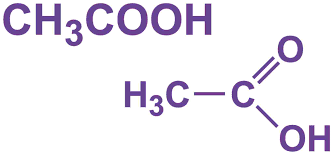
Axit axetic có thể được nhận biết bởi mùi đặc trưng của nó. Phản ứng biến đổi màu đối với các muối của axit axetic là cho tác dụng với dung dịch sắt(III) chloride, phản ứng này tạo ra màu đỏ đậm sau khi axit hóa. Khi nung nóng các axetat với arsen trioxit tạo ra cacodyl oxit, chất này có thể được nhận biết bởi các hơi có mùi hôi.
Phương trình phản ứng đã cân bằng :
CH3COOH + 2O2 → 2H2O + 2CO2
Trong đó :
CH3COOH : dung dịch axit axetic
O2 : là chất khí không màu
H2O : nước là chất lỏng không màu
CO2 : là khí Cacbon dioxit không màu
Khi phản ứng xảy ra chúng ta cần có sự can thiệp của nhiệt độ thường.
Cách thực hiện phản ứng:
Đốt cháy CH3COOH trong không khí.
Hiện tượng xuất hiện : ta thấy có khí thoát ra ngoài.
Điều chế, sản xuất CH3COOH axit axetic như thế nào?
Axit Axetic CH3COOH được điều bằng các phương pháp quen thuộc dưới đây:
a, Điều chế bằng cách cacbonyl hóa metanol
Ta cho metanol và cacbon monoxit phản ứng với nhau sẽ tạo ra axit aextic:
CH3OH + CO → CH3COOH
b, Oxy hóa axetaldehyt để điều chế CH3COOH
Axetaldehyt có thể bị oxy hóa bởi oxy trong không khí, để tạo ra axit axetic dưới tác dụng của những điều kiện xúc tác (sự có mặt các ion kim loại: mangan, coban, và crôm, peroxit).
2 CH3CHO + O2 → 2 CH3COOH
c, Oxy hóa etylen
Quá trình này sử dụng chất xúc tác là kim loại palladi với sự hỗ trợ của axit heteropoly như axit tungstosilicic.
Đây là một phương pháp có thể cạnh tranh với phương pháp cacbonyl hóa metanol đối với các nhà máy nhỏ hơn (100–250 ngàn tấn/năm), tùy thuộc vào giá của etylen.
d, Lên men oxy hóa của CH3COOH
Khi cung cấp đủ oxy, các vi khuẩn này có thể tạo ra giấm từ các thực phẩm sinh cồn khác nhau như rượu táo, rượu vang hay các loại ngũ cốc (gạo, mạch nha hoặc khoai tây) lên men.
C2H5OH + O2 → CH3COOH + H2O
e, Lên men kỵ khí để sản xuất axit axetic
Các loài vi khuẩn kỵ khí bao gồm cả thuộc chi Clostridium, có thể chuyển đổi đường thành axit axetic một cách trực tiếp mà không cần phải qua bước trung gian: C6H12O6 → 3 CH3COOH
Xem thêm các phương trình phản ứng hóa học cân bằng :
3K2CO3 + 2H3PO4 → 3H2O + 2K3PO4 + 3CO2
CH3OH CO2 viết phương trình phản ứng hóa học