Cấu hình electron của nguyên tử cho ta biết: sự phân bố electron trên các lớp và phân lớp. Qua cấu hình electron ta biết được cấu tạo nguyên tử, vị trí của nguyên tố trong bảng tuần hoàn và tính chất hóa học đặc trưng của nguyên tố đó. Một khi hiểu được các nguyên lý cơ bản của cấu hình electron, bạn sẽ tự viết được cấu hình electron và có thể làm các bài kiểm tra hóa học một cách tự tin.
Thứ tự các mức năng lượng trong nguyên tố :
Các electron trong nguyên tử
ở trạng thái cơ bản lần lượt chiếm các mức năng lượng từ thấp đến cao.
Từ trong ra ngoài, mức năng lượng của các lớp tăng theo thứ tự từ 1 đến 7 và năng lượng của phân lớp theo thứ tự s, p, d, f 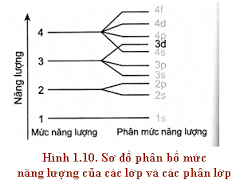
Khi điện tích hạt nhân tăng, có sự chèn mức năng lượng nên mức nặng lượng 4s thấp hơn 3d
Cấu hình Electron của nguyên tử :
1. Cấu hình electon nguyên tử
Cấu hình electron nguyên tử biểu diễn sự phân bố electron trên các phân lớp thuộc các lớp khác nhau.
Quy ước cách viết cấu hình electron nguyên tử:
– Số thứ tự lớp electron được ghi bằng chữ số (1, 2, 3…)
– Phân lớp được ghi bằng các chữ cái thường (s, p, d, f).
– Số electron trong một phân lớp được ghi bằng số ở phía trên bên phải của phân lớp.
Cách viết cấu hình electron nguyên tử gồm các bước sau:
Xác định số electron của nguyên tử.
Các electron được phân bố lần lượt vào các phân lớp theo chiều tăng của năng lượng trong nguyên tử và tuân theo quy tắc sau: phân lớp s chứa tối đa 2 electron; phân lớp p chứa tối đa 6 electron, phân lớp d chứa tối đa 10 electron; phân lớp f chứa tối đa 14 electron.
Viết cấu hình electron biểu diễn sự phân bố electron trên các phân lớp thuộc các lớp khác nhau.
Ví dụ: Nguyên tử Fe có Z= 26.
+ Có 26e
+ Các e được phân bố như sau: 1s2 2s2 2p6 3s2 3p6 4s2 3d6. Có sự chèn mức năng lượng 4s < 3d
+ Sắp xếp lại các phân lớp theo từng lớp, ta được cấu hình e: 1s2 2s2 2p6 3s2 3p6 3d6 4s2
Hoặc viết gọn: [Ar] 3d6 4s2 ( [Ar] là cấu hình electron nguyên tử của nguyên tố argon, là khí hiếm gần nhất đứng trước Fe )
Nguyên tố s là những nguyên tố mà nguyên tử electron cuối cùng được điền vào phân lớp s
Nguyên tố p là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp p
Nguyên tố d là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp d
Nguyên tố f là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp f

2.Cấu hình ELECTRON nguyên tử của 20 nguyên tố đầu :

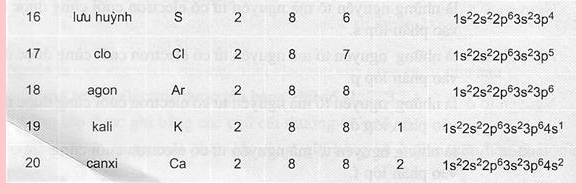
3.Đặc điểm của lớp electron ngoài cùng:
– Đối với nguyên tử của tất cả các nguyên tố, lớp electron ngoài cùng có nhiều nhất là 8 electron.
– Các nguyên tử có 8 electron ở lớp electron ngoài cùng (ns2np6) và nguyên tử heli (1 s2) không tham gia vào các phản ứng hoá học (trừ trong một số điều kiện đặc biệt) vì cấu hình electron của các nguyên tử này rất bền. Đó là các nguyên tử của nguyên tố khí hiếm. Trong tự nhiên, phân tử khí hiếm chỉ có một nguyên tử.
– Các nguyên tử có 1, 2, 3 electron ở lớp ngoài cùng dễ nhường electron là nguyên tử của các nguyên tố kim loại (trừ H, He và B).
– Các nguyên từ có 5, 6, 7 electron ở lớp ngoài cùng dễ nhận electron thường là nguyên tử của nguyên tố phi kim.
– Các nguyên từ có 4 electron ngoài cùng có thể là nguyên tử của nguyên tố kim loại hoặc phi kim
Sơ đồ tư duy: Cấu hình electron nguyên tử
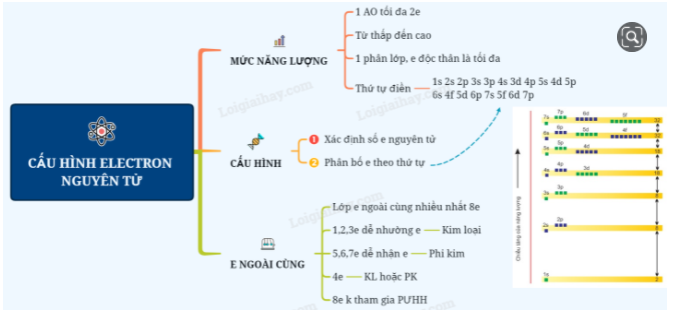
Bài tập vận dụng :
Bài 1 :
Viết cấu hình electron của nguyên tử các cặp nguyên tố mà hạt nhân nguyên tử có số proton là :
a) 1, 3; b)8, 16; c) 7, 9.
Những nguyên tố nào là kim loại ? Là phi kim ? Vì sao ?
Hướng dẫn Giải bài 1:
Hạt nhân nguyên tử cho biết số proton (nghĩa là cho biết số đơn vị điện tích hạt nhân) nên theo yêu cầu của đề bài ta có thế viết cấu hình electron của nguyên tử các cặp nguyên tố như sau :
a) z = 1 : 1s1 ; z = 3 : 1s2 2S1 ;
b) z = 8 : 1s2 2s2 2p4 ; z = 16 : 1s2 2s2 2p6 3s2 3p4 ;
c) z = 7 : 1s2 2s2 2p3 ; z = 9 : 1s2 2s2 2p5.
Nguyên tố kim loại có 1, 2, 3 electron lớp ngoài cùng, nên nguyên tố có z = 3 là kim loại, còn nguyên tố z = 1 là H giống kim loại nhưng không phải là kim loại.
Nguyên tố phi kim có 5, 6, 7 electron ở lớp ngoài cùng nên các nguyên tô có z = 8, z = 16, z = 7, z = 9 là phi kim.
Bài 2:
Tổng số hạt proton, nơtron và electron trong nguyên tử của một nguyên tố là 13.
a) Xác định nguyên tử khối.
b) Viết cấu hình electron nguyên tử của nguyên tố đó.
(Cho biết : các nguyên tô cỏ sô hiệu nguyên tử từ 2 đến 82 trong N bảng tuần hoàn thì 1 ≤ N/Z ≤ 1,5)
Hướng dẫn Giải bài 2:
a) Tổng số hạt proton, nowtron, electron trong 1 nguyên tử của nguyên tố đã cho là 13. Mà số proton bằng số electron nên ta có phương trình sau:
2Z + N =13
Mặt khác từ nguyên tố số 2 đến 82 trong bảng tuần ta có :
Z ≤ N; mà N =13 – 2Z ⇒ Z ≤ 13 – 2Z ⇒ Z ≤ 4,333 (1)
N ≤ 1,5Z ⇒ 13-2Z ≤ 1,5Z ⇒ 3,5Z ≥ 13 ⇒ Z ≥ 3,7 (2)
Từ (1) và (2) và vì Z nguyên dương 3,7 ≤ Z ≤ 4,333 . vậy Z =4
Suy ra số nơtron: N =13 – 2Z = 13 -2.4 = 5
Vậy nguyên tử khối cần tìm theo yêu cầu bài toán là 4+5=9.
b) Viết cấu hình electron: Z=4 có cấu hính là 1s22s2. Đây là nguyên tố s
Xem thêm : Cấu tạo vỏ nguyên tử, chuyển dộng Electron
Hạt nhân nguyên tử, nguyên tố hóa học và đồng vị
Thành phần cấu tạo,kích thước và khối lượng của nguyên tử