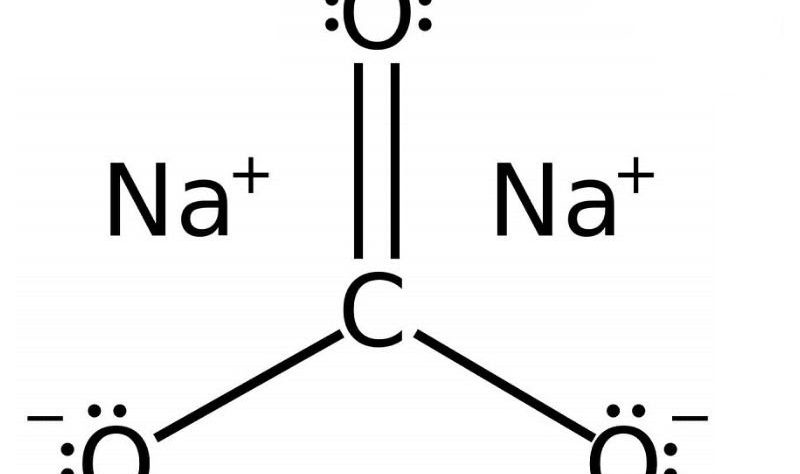
Na2CO3 ⟶ Na2O + CO2 Cân bằng phương trình phản ứng của muối Natri Cacbonat sau khi đã cân bằng. Vì là một bazơ mạnh, natri hydroxit trung hòa axit dạ dày, do đó hoạt động như một chất kháng axit. Natri cacbonat là muối dinatri của axit cacbonic với đặc tính kiềm hóa. Khi hòa tan trong nước, natri cacbonat tạo thành axit cacbonic và natri hiđroxit. Ở bài này chúng tôi sẽ giới thiệu cũng như hướng dẫn các bạn cách cân bằng phương trình và các phương trình điều chế Na2CO3, Các bạn cùng chú ý đón đọc.

Na2CO3 khan là chất bột màu trắng, hút ẩm và nóng chảy ở 851 °C, nóng chảy không phân hủy tới 853 °C, còn cao hơn nhiệt độ này thì bắt đầu phân hủy. Chất dễ tan trong nước, khi tan trong nước phát ra nhiều nhiệt do tạo thành hiđrat.
Cân bằng phương trình Na2CO3 :
Na2CO3 ⟶ Na2O + CO2
Trong đó :
Na2CO3 : là Muối natri cacbonat chất rắn có màu trắng
Na2O : là natri oxit chất rắn màu trắng
CO2 : là khí Cacbon dioxit không màu
Khi gặp nhiệt độ cao > 1000 độ thì xảy ra nhanh, Phản ứng xảy ra chậm ở điều kiện thường
Cách thực hiện phản ứng
Cho 1 lượng nhỏ natri cacbonat vào ống nghiệm, dùng kẹp gỗ cặp ống nghiệm rồi đun nóng trên ngọn lửa đèn cồn
Quan sát thí nghiệm ta thấy hiện tượng không xảy ra.
Thông tin thêm
Muối natri cacbonat không thể tham gia phản ứng phân hủy tạo thành natri oxit và khí CO2 giống như một số muối cacbonat khác, chẳng hạn như CaCO3, BaCO3,… Phản ứng phân hủy là phản ứng hóa học trong đó một chất sinh ra hai hoặc nhiều chất mới.
Các phương trình điều chế Na2CO3:
NaHCO3 + NaOH —> H2O + Na2CO
Na2CO3.10H2O —> 10H2O + Na2CO3
NaOH + C6H4CH3COONa —> Na2CO3 + C6H5CH3
CO2 + Na2N2O2 —> N2O + NaCO3
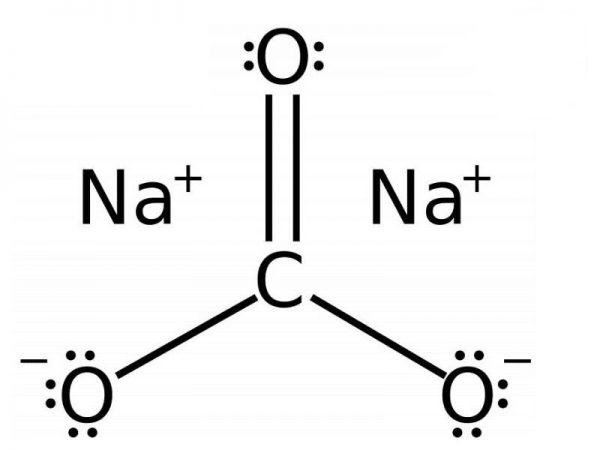
Các tính chất của Na2CO3:
Tác dụng với axít tạo thành muối, nước và giải phóng khí CO2
Na2CO3 + HCl → NaCl + NaHCO3
Khi Axit dư thì
Na2CO3 + HCl → NaCl + Co2 + H20
Tác dụng với bazơ tạo thành muối mới và bazơ mới
Na2CO3 + NaOH → NaCO3 + Na2OH
Tác dụng với muối tạo thành 2 muối mới
Na2CO3 + CaCl2 → 2NaCl + CaCO3
Tác dụng chuyển đổi qua lại với natri bicacbonat theo phản ứng
Na2CO3 + CO2 + H2O = 2NaCl + CaCO3
Ngoài ra hóa chất này không bị nhiệt phân hủy ở nhiệt độ cao và làm quỳ tím chuyển sang màu xanh
Xem thêm cân bằng phương trình phản ứng :