Kali và natri có tính chất hóa học rất giống nhau, đều là những nguyên tố nhóm IA trong bảng tuần hoàn. Chúng có cùng mức năng lượng ion hóa thứ nhất, khi được kích hoạt thì nguyên tử của hai nguyên tố này sẽ cho đi electron ngoài cùng duy nhất. Dù là hai nguyên tố khác nhau, nhưng kali và natri có thể kết hợp với những anion giống nhau để tạo nên những muối có tính chất tương tự, để hiểu rõ nguyên tố này thì chúng ta đi tìm hiểu Nguyên tử khối của Kali là bao nhiêu? Kali ( K ) hóa trị mấy ? Các bạn có thể xem chi tiết Kali là gì? Để giải phương trình hóa học chính xác.
Nguyên tử khối của Kali là bao nhiêu? Kali ( K ) hóa trị mấy ?

– Kali kí hiệu là: K
– Kali vị trí trong bảng tuần hoàn
+ Số proton : 19
+ Nhóm : IA
+ Chu kì : 4
+ Kali hóa trị : I
+ Nguyên tử khối Kali : 39
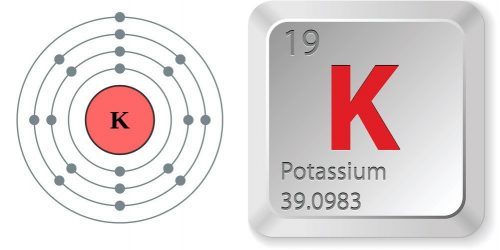
– Cấu hình electron : [ Ar ] 4 s1
– Số hiệu nguyên tử K : 19
– Khối lượng nguyên tử : 39 g / mol
– Đồng vị K : 39K, 40K, 41K .
– Độ âm điện K : 0,82
Tính chất vật lí:
– Kali là kim loại nhẹ thứ hai sau liti, là chất rắn rất mềm, dễ dàng cắt bằng dao và có màu trắng bạc.
– Kali bị ôxi hóa rất nhanh trong không khí và phải được bảo quản trong dầu mỏ hay dầu lửa.
Có khối lượng riêng là 0,863 g/cm3; có nhiệt độ nóng chảy là 63,510C và sôi ở 7600C.
- Clo ( Cl ) hóa trị mấy? Nguyên tử khối của Cl
- CO3 hóa trị mấy? Phân tử khối và Cách nhận biết ion CO3
- Kẽm ( Zn ) hóa trị mấy? tính chất hóa học và vai trò của Zn
Nhận biết
– Đốt cháy các hợp chất của Kali, cho ngọn lửa màu tím.
Các hợp chất quan trọng của Kali
– Kali hiđroxit: KOH
Tính chất hóa học
– K có tính khử rất mạnh.
a. Tác dụng với phi kim
Ví dụ: 4K + O2 → 2K2O
2K + Cl2 → 2KCl
– Khi đốt trong không khí hay trong oxi, kali cháy tạo thành các oxit (oxit thường, peoxit và supeoxit) và cho ngọn lửa có màu tím hoa cà đặc trưng.
b. Tác dụng với axit
– Kali dễ dàng khử ion H+ (hay H3O+) trong dung dịch axit loãng (HCl, H2SO4 loãng…) thành hidro tự do.
Ví dụ: 2K + 2HCl → 2KCl + H2.
c. Tác dụng với nước

– K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
d. Tác dụng với hidro
Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
Điều chế
– Kali có thể cô lập bằng điện phân của hiđrôxít của nó trong một quy trình có một chút thay đổi kể từ thời của Davy.
K (-) KOH n/c A (+)
K+ + e → K 4OH- – 4e → O2 + 2H2O
Phương trình điện phân:
4KOH n/c→ 4K + O2 + 2H2O
Trạng thái tự nhiên
– Dạng tự nhiên của K có 3 đồng vị : K39 ( 93,3 % ), K40 ( 0,01 % ) và K41 ( 6,7 % ) .
– Nguyên tố này chiếm khoảng chừng 2,4 % khối lượng lớp vỏ Trái Đất và là nguyên tố phổ cập thứ bảy trong lớp này. Vì tính không hòa tan của nó, rất khó thu được kali từ những khoáng chất của nó .
Ứng dụng của Kali :
– Các loại phân hóa học chứa kali như clorua kali, sulfat kali, cacbonat kali v.v được tính hàm lượng quy đổi theo Xác Suất K2O. Các ứng dụng khác .
+ Nitrat kali được sử dụng trong thuốc súng .
+ Cacbonat kali được sử dụng trong sản xuất thủy tinh .
+ Thủy tinh được giải quyết và xử lý bằng kali lỏng là có độ bền cao hơn so với thủy tinh thường .
+ NaK là kim loại tổng hợp của kali với natri được sử dụng như là chất truyền nhiệt trung gian .
+ Nguyên tố này là thành phần rất thiết yếu cho sự tăng trưởng của cây cối và được tìm thấy trong nhiều loại đất .
Xem thêm bảng hóa trị và hóa trị của các nguyên tố :
Bảng Hóa Trị Lớp 8, Cách Học Thuộc Bằng Bài Ca Hóa Trị Hóa Học.
Brom ( Br ) hóa trị mấy? Nguyên tử khối của Brom là bao nhiêu?
OH hóa trị mấy? Nguyên tử khối của M trong hidroxit M(OH)3
Hóa trị Bari ( Ba ) là mấy? Nguyên tử khối của Ba
SO3 hóa trị mấy? Công thức cấu tạo và tính chất hóa học của SO3